第4章 大気と海の歴史
1. 大気の変遷
a.酸素
はじめ、地球の大気には酸素がなかった。あるいはほとんどなかった。大気中の酸素は、生物が作り出し、それがたまりにたまってできたものである。現在の地球の大気組成は体積百分率で、ちっ素が78%、酸素が21%、アルゴンが0.93%、この3つでほとんどを占める。二酸化炭素は約0.03%程度とごくわずかでしかない。
生物とは無関係に酸素ができることもある。酸素は上空に昇った水蒸気が、太陽光の中の紫外線によって分解することによってもできる。だが、その量は大変に少なく、大気圧に換算して1hPa(1ヘクトパスカル、1Pa=1N・m-2、1気圧≒10万Pa、100Pa=1hPa(ヘクトパスカル)、だから1hPaは約10-3気圧)程度でしかない。現在の地球の大気圧は1013hPa、酸素はその20%なので200hPaもある。逆にいえば、こうした反応では現在の酸素の量の1/200程度しかできない。
だから酸素を作り出すメカニズムは植物の光合成である。光合成は模式的に下のように書ける。
6CO2 + 6H2O + 光 → C6H12O6 + 6O2 (C6H12O6はデンプン)
光合成を行うシアノバクテリア(ランソウ、らん藻)は少なくとも28億年前、もしかすると35億年前にはすでに登場していたと考えられている。
こうしてできた酸素は、まず地表を酸化させることで消費されてしまう。古い時代の地層からは赤色土層(赤鉄鉱(Fe2O3))というものが見られる。この赤色土層の一番古いものは24億年前のものという。ただし、確実なものは20億年前のものという。
22億年前〜19億年前になると、縞状鉄鉱層(縞状鉄鉱床)が大量に形成されるようになる。縞状鉄鉱層は鉄の酸化物を大量に含むもので、現在の世界中の鉄鉱石の90%以上を供給している。この縞状鉄鉱層は19億年以降はほとんど見られなくなる。つまり、このころまでは植物がつくる酸素は、鉄などを酸化させることに消費され、大気中にはあまりたまらなかったかもしれない。しかし、こうした出来事(酸化されやすいものの酸化)が終わると大気中に酸素が急にたまり出す。
こうしてできた酸素は、生物の体を作る有機物にとっては危険な存在である。しかし、酸素を利用(呼吸)することによってエネルギーの生成が効率的にできる。つまり、大気中の酸素濃度と生物の進化は関係しているとも考えられる。細胞の中に核を持つ真核生物は、ある程度高い酸素濃度を必要とする。またそもそも真核生物のミトコンドリアは、酸素を使ってエネルギーを得る器官である。一番古い確実な真核生物の化石は約21億年前である。こうしたことについては、生命の進化(真核生物への進化)も参照。
また、6億年前には多細胞生物が登場する。これも酸素濃度の増加に関係しているのかもしれない。さらに、4億年前には陸上で生活する生物も登場する。これは、大気中の酸素濃度が十分に高くなり、それに伴って成層圏のオゾン濃度も高くなったことを示すのかもしれない。成層圏のオゾンは、生物(とくに遺伝をつかさどるDNA)を損傷する、生物にとっては有害な太陽からの紫外線を有効に吸収する。これについてはこちらを参照。こうした出来事が、どの程度の酸素濃度を示すものかはよくわからない。
4億年前の生物の上陸以降は、森林火災の化石(木炭化石)が出ることから大気中の酸素濃度は13%以上、自然発火により森林が全焼したことがないということから35%以上にはなったことがないだろうといわれている。約3億年前の酸素濃度はその上限(現在の約1.5倍)に達し、巨大な昆虫(もちろん「風の谷のナウシカ」に登場するような超巨大昆虫ほどではないが、翼開長70cm程度のトンボなど)の存在を許したともいわれている。
生物の進化と酸素の関係についてはこちらも参照。
b.二酸化炭素
原始地球の大気中の二酸化炭素濃度は、現在よりもはるかに高かった考えられている。また大気中の二酸化炭素は地球の温度を決める上で重要な役割を果たす。
主系列星として核融合反応をはじめたころ太陽は、現在の光度よりも25%〜30%程度暗かったという。そしてだんだんと明るくなり、現在の姿になったらしい。大気中の二酸化炭素が現在の濃度だと、暗い太陽のもとでは当然温度も低く、20億年前までは全球凍結(地球表面では液体の水は存在しない状態)になっていなくてはならない。一方、少なくとも38億年前の年齢を示す、堆積岩起源(つまり海があった)の変成岩が存在する。これが、「暗い太陽のパラドックス(逆説)」である。
一番簡単な解決は、昔は二酸化炭素の濃度は高かったとするものである。そして、太陽の光度が増すにつれ、大気中の二酸化炭素は地殻に固定され、長期的にはじょじょに減っていったのだろう。ただし、かなり大きな「ゆらぎ」もあり、過去に何回か二酸化炭素濃度が小さくなり、全球凍結の時代もあったらしい。また、逆に中生代(恐竜が反映した時代、約2億年前〜1億年前)は、大気中の二酸化炭素濃度が高く、現在よりもかなり暖かかったらしい。
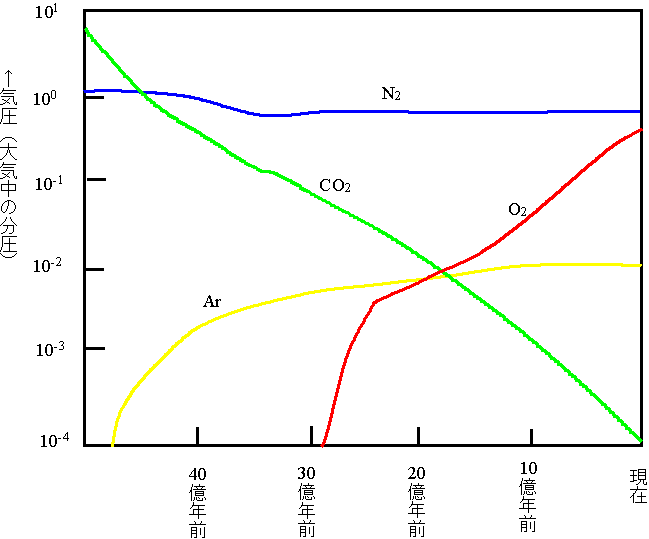
大気の変遷の推定例を下に示す。地球の歴史を通じて二酸化炭素(CO2)は減少し、酸素(O2)は増大、アルゴン(Ar)もたまってくる、またちっ素(N2)はそれほど変化がない(結果として現在の地球大気に主成分となる)ことがわかる。

「地球の進化」(岩波地球惑星科学13)の図5.16より作成
下に、過去6億年間における酸素(O2)と二酸化炭素(CO2)の量の変化の推定例を示す。細かく見ると、酸素や二酸化炭素の量にはかなりの変動があったことになる。
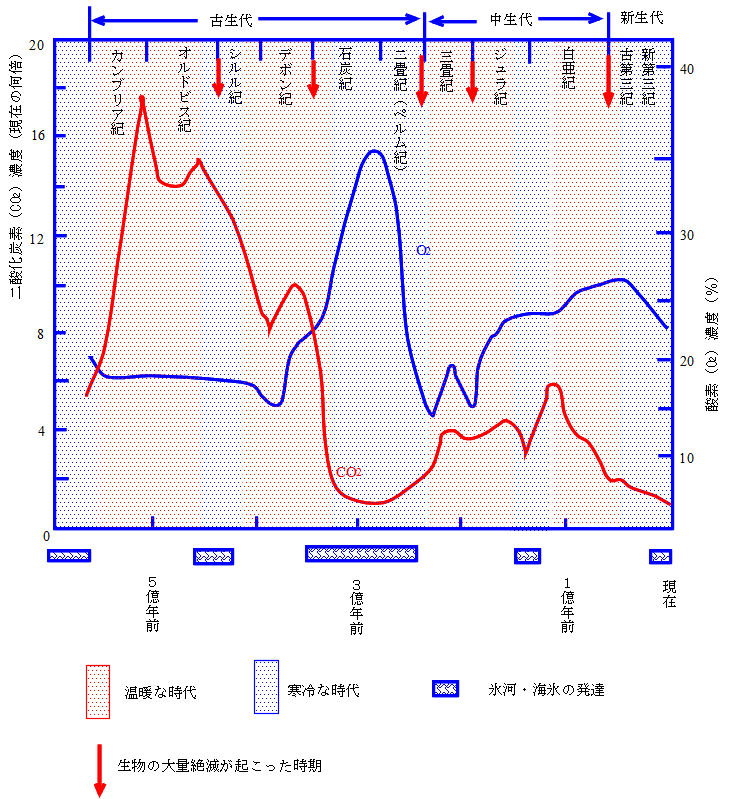
「地球の進化」(岩波地球惑星科学講座13,1998年)の図6.15より作成。
なお、大気中の二酸化炭素の増減の問題についてはこちらも参照。
2. 海水の変遷
大気と同じく、昔の海水もそのままでは残らないので、過去の海水の組成の推定は難しい。
海水中のイオンの組成とその濃度は、河川とはまったく異なっている。また、平均滞留時間は、地球の歴史と比べても極めて短い。つまり、海水のイオンは河川が運び込んできたものがそのままたまったものではない。
海水中の水(H2O)と陰イオン(Cl-、SO42-、HCO3-など)は、原始地球時代の脱ガスやその後の火成活動(火山ガス)で供給されてきたものである。一方、陽イオン(Na+、K+、Mg2+、Ca2+など)は、初めは強酸性であった可能性がある海水が地殻(岩石)を溶かしたもの、さらにはその後の陸上や海底での風化作用(水にごくわずかずつ溶ける)に供給されてきたものである。
少なくとも過去数億年前から現在までは、河川が海に運び込むイオンと同じ量がそっくり沈殿し、海水の組成はほとんど変化しなくなっていると考えられている。生物の体液の組成が海水の組成と似ていることは、生物が発生したころの海水の組成が現在と似ていたことを示しているのかもしれない。
海水の量の変化もよくわかっていない。地球初期の大規模な脱ガスにより、ほとんど現在の量の水(H2O)が供給されたという可能性が高いという。
ではその後の脱ガス(火山ガス)により、現在も海水がじょじょに増加しているかというとこれまた難しい。中央海嶺からはH2Oは1.1×1011kg・年-1、ホットスポットからは0.13×1011kg・年-1の、合計1.2×1011kg・年-1が供給されているという。そして、地球の歴史を通じては、(0.76〜1.18)×1021kgのH2Oが脱ガスしたという。これは、現在の海水量の54%〜84%になる。これだけだと地球の歴史を通じて、海水の量は2倍程度に増えたことになる。
しかし一方、海洋プレートの沈み込みにより、H2Oがマントルに運ばれている。海洋地殻では、中央海嶺の熱水活動により水を含んだ岩石が存在し、また海洋底には水を大量に含んだ堆積物が存在する。これらが海洋プレートによってマントルに運ばれるが、その量は9.7×1011kg・年-1と考えられている。こうしたH2Oはすべてがマントルに入り込むのではなく、日本のような弧状列島の火山活動により脱ガスするものある。その量は1.0×1011kg・年-1と考えられている。正味では約8×1011kg・年-1の割合で、地表からマントルへH2Oが運ばれていることになる。
これらが正しいとすると、脱ガス(1.2×1011kg・年-1)よりも、マントルに運び込まれるH2O(8×1011kg・年-1)の方が圧倒的に多いことになる。つまり、このままではあと20億年程度で海水は消滅することになる。現在の海水の量を説明するためには、過去には現在の2倍〜3倍程度の海水があったとする考えもある。
このように、地表と地球内部での水循環により、海水の量はかなり変化した可能性がある。そしてそれはまた、地表や地球内部の状態、脱ガスの組成に対して大きな影響があるが、詳しいことはよくわかっていない。
酸素の生成:水蒸気は紫外線によって、
H2O + 紫外線 → 2H + O と分解する。
このO(原子酸素)は
O + O + M → O2 + M (Mは触媒、Nなどがその役割を果たす)
O2 + O + M → O3 + M
O + O3 → 2O2
こうしてO2はできるが、そのO2も水蒸気と同じように紫外線を吸収して、
O2 + 紫外線 → O + O
となってしまう。
こうして、大気中のO2は1hPa程度しかたまらない。
バクテリアの働き:生物が酸素をつくるもう一つは硫酸還元バクテリアである。海における黄鉄鉱生成には硫酸還元バクテリアが関係しており、その黄鉄鉱が埋没することにより、酸素が放出されることになる。
呼吸:呼吸は光合成の逆反応で、デンプン(炭素の高分子=有機物)を酸素を使って分解し、生存のためのエネルギーを得るものである。
C6H12O6 + 6O2 → 6CO2 + 6H2O + エネルギー
大きく見れば現在は、生物が生産する酸素と、生物が消費する酸素が釣り合い、極端な酸素濃度の変化はないと考えられている。
パストゥール点(PAL):酸素を使う呼吸と、使わない呼吸のどちらが有利かの境目。10hPa(10-2気圧)よりも酸素濃度が高いと酸素を利用した呼吸が有利(好気的代謝)、酸素濃度が10hPaよりも小さいと酸素を使わない発酵(嫌気的代謝)が有利になる。この境目の10-2気圧(10hPa)をパストゥール点(PAL)という。
海水中のイオン濃度:下の表は「地球進化論」(岩波地球惑星科学講座13、1998年1月)による。海水中の塩分量についてはこちらも参照。また、海水中の塩分の起源についてはこちらも参照。
| 溶存イオン | 海水中の濃度(103mol・L-1) | 河川水中の濃度(103mol・L-1) | 平均滞留時間(106年) |
| Na+ | 479.0 | 0.315 | 55 |
| K+ | 54.3 | 0.036 | 10 |
| Mg2+ | 10.5 | 0.150 | 13 |
| Ca2+ | 10.4 | 0.367 | 1 |
| Cl- | 558.0 | 0.230 | 87 |
| SO42- | 28.9 | 0.120 | 8.7 |
| HCO3- | 2.0 | 0.870 | 0.083 |
ヒトの血液と海水:下の表は「海のはなしII」(技報堂出版、1984年)より作成した。海水に多いものは血液にも多いことがわかる。ただし、全体として血液の方が海水よりも塩分濃度では1/3程度に薄くなっている。
| イオン | 海水(g・L-1) | 血液(血清)(g・L-1) |
| ナトリウム | 10.9 | 3.3 |
| マグネシウム | 1.3 | 0.1 |
| カルシウム | 0.4 | 0.1 |
| カリウム | 0.4 | 0.2 |
| 塩素 | 19.6 | 3.7 |